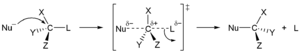विन्यास का प्रतिलोमन: Difference between revisions
m (added Category:उपसहसंयोजक यौगिक using HotCat) |
No edit summary |
||
| (8 intermediate revisions by 2 users not shown) | |||
| Line 1: | Line 1: | ||
[[Category:रसायन विज्ञान]] | [[Category:हैलोएल्केन तथा हैलोएरीन]][[Category:रसायन विज्ञान]][[Category:कक्षा-12]][[Category:कार्बनिक रसायन]] | ||
[[Category:कार्बनिक रसायन]] | विन्यास का प्रतिलोमन स्टीरियोकेमिस्ट्री में एक महत्वपूर्ण अवधारणा है जो रासायनिक अभिक्रिया के दौरान एक [[काइरल]] केंद्र के आसपास परमाणुओं की स्थानिक व्यवस्था में परिवर्तन को संदर्भित करता है, जिसके परिणामस्वरूप मूल [[अणु]] के एक एनैन्टीओमर का निर्माण होता है। यह अवधारणा सामान्यतः न्यूक्लियोफिलिक [[प्रतिस्थापन अभिक्रिया]]ओं, विशेषकर SN<sub>2</sub> में पाई जाती है | ||
[[ | |||
== क्रियाविधि == | |||
=== विन्यास के प्रतिलोमन को समझना === | |||
=== काइरल केंद्र === | |||
एक कार्बन परमाणु चार अलग-अलग समूहों से बंधा होता है, जिससे गैर-सुपरइम्पोज़ेबल दर्पण छवियां (एनेंटिओमर्स) बनती हैं। रसायन विज्ञान में, कोई अणु या [[आयन]] काइरल तब कहलाता है यदि वह अणु और उसका दर्पण-प्रतिबिम्ब एक दूसरे को पूर्णतया 'ढक' न सकें। काइरलता एक अणु, आयन या किसी वस्तु में विषमता का गुण है। एक काइरल अणु वह है जिसे उसकी दर्पण छवि पर आरोपित नहीं किया जा सकता है। शब्द "काइरलता" ग्रीक शब्द "चीर" से आया है, जिसका अर्थ है "हाथ", क्योंकि काइरल अणु को प्रायः बाएं या दाएं हाथ की तरह वर्णित किया जाता है - दर्पण छवियां जिन्हें आरोपित नहीं किया जा सकता है। | |||
'''''[[काइरलता]] को समरूपता की कुछ विशेषताओं की कमी से परिभाषित किया गया है, जिसके कारण कोई वस्तु अपनी दर्पण छवि पर आरोपित नहीं हो पाती है। हैंडेडनेस काइरल वस्तुओं को दाएं हाथ और बाएं हाथ की वस्तुओं में वर्गीकृत करने की क्षमता से संबंधित एक अलग घटना है।''''' | |||
===काइरल अणु=== | |||
एक अणु काइरल है यदि इसमें समरूपता का आंतरिक तल नहीं है। दूसरे शब्दों में, इसकी दर्पण छवि को मूल अणु पर आरोपित नहीं किया जा सकता है। काइरलता स्टीरियोकेमिस्ट्री के क्षेत्र में एक महत्वपूर्ण अवधारणा है, जो अणुओं में परमाणुओं की त्रि-आयामी व्यवस्था का अध्ययन करती है। | |||
=== न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया === | |||
एक अभिक्रिया जहां एक न्यूक्लियोफाइल कार्बन परमाणु से जुड़े एक छोड़ने वाले समूह को प्रतिस्थापित करता है। CH<sub>3</sub>Cl और हाइड्रॉक्साइड आयन की अभिक्रिया, जिसमें मेथेनॉल तथा क्लोराइड आयन बनता है यह एक द्वितीयक कोटि की अभिक्रिया है। अर्थात, अभिक्रिया का वेग दोनों अभिकारकों की सांद्रता पर निर्भर करता है। इस अभिक्रिया को आरेखीय रूप में भी प्रदर्शित किया जा सकता है। | |||
<chem>OH- + CH3Cl -> [OH...CH3...Cl] -> CH3-OH + Cl-</chem> | |||
*प्रतिस्थापन न्यूक्लियोफिलिक बिमोलेक्यूलर (SN<sub>2</sub>) अभिक्रिया एक प्रकार की कार्बनिक रासायनिक अभिक्रिया है जहां एक न्यूक्लियोफाइल (इलेक्ट्रॉन-समृद्ध प्रजाति) एक अणु में एक वाले समूह को प्रतिस्थापित करती है, जिससे एक नए रासायनिक बंध का निर्माण होता है। "द्विआणविक" पहलू इस तथ्य को संदर्भित करता है कि अभिक्रिया के दर-निर्धारण चरण में दो अणुओं का टकराव सम्मिलित है। | |||
*SN<sup>2</sup> अभिक्रियाएं स्टीरियोस्पेसिफिक होती हैं, जिसका अर्थ है कि वे प्रतिस्थापन के दौर से गुजर रहे कार्बन केंद्र में स्टीरियोकैमिस्ट्री के व्युत्क्रम के साथ आगे बढ़ती हैं। ऐसा इसलिए होता है क्योंकि न्यूक्लियोफाइल छोड़ने वाले समूह के विपरीत पक्ष से हमला करता है, जिससे कॉन्फ़िगरेशन का सीधा उलटा होता है। | |||
*न्यूक्लियोफाइल इलेक्ट्रोफिलिक कार्बन परमाणु पर उस समय हमला करता है जब निकलने वाला समूह प्रस्थान करता है। इसका परिणाम एक संक्रमण अवस्था में होता है जहां न्यूक्लियोफाइल और छोड़ने वाला समूह दोनों आंशिक रूप से केंद्रीय कार्बन [[परमाणु]] से बंधे होते हैं। | |||
==अभिक्रिया दर== | |||
[[File:SN2 reaction mechanism.png|thumb|द्विआणविक प्रतिस्थापन अभिक्रिया]]SN<sup>2</sup> अभिक्रियाओं की दर न्यूक्लियोफाइल और सब्सट्रेट दोनों की सांद्रता पर निर्भर करती है, साथ ही अभिक्रियाशील कार्बन परमाणु के आसपास स्टेरिक बाधा पर भी निर्भर करती है। सामान्यतः SN<sup>2</sup> अभिक्रिया धीमी गति से गुजरते हैं। | |||
द्विअणुक नाभिकरागी प्रतिस्थापन को प्रदर्शित करता है। आक्रमणकारी नाभिकरागी की एल्किल हैलाइड से अन्योन्य क्रिया होने पर कार्बन और हैलोजन के मध्य का बंध टूटता है तथा कार्बन एवं आक्रमणकारी नाभिकरागी के मध्य एक नया आबंध बनता है। ये दोनों प्रक्रियाएं एक साथ एक ही पद में संपन्न होती हैं तथा कोई मध्यवर्ती नहीं बनता। जब अभिक्रिया प्रगति है तब आने वाले नाभिकरागी एवं कार्बन परमाणु के मध्य आबंध बनना प्रारम्भ हो जाता है। फिर क्रियाधार के कार्बन हाइड्रोजन बंध आक्रमणकारी नाभिकरागी से लगते हैं जब नाभिकरागी कार्बन के समीप पहुँचता है तब बंध पहले की दिशा में अग्रसर होते रहते हैं जब तक टूटने वाला समूह कार्बन से टूटकर अलग नहीं हो जाता परिणामस्वरूप आक्रमण के लिए उपलब्ध कार्बन परमाणु का विन्यास पलट जाता है और अवशिष्ट समूह बाहर निकल जाता है। इस प्रक्रिया को विन्यास का प्रतीपन कहते हैं। | |||
विन्यास का प्रतिलोमन तब होता है जब एक रासायनिक अभिक्रिया के दौरान एक काइरल केंद्र के चारों ओर परमाणुओं की स्थानिक व्यवस्था उलट जाती है। SN<sup>2</sup> तंत्र, यह उलटा न्यूक्लियोफाइल के पीछे के हमले के कारण होता है, जिसके परिणामस्वरूप विपरीत एनैन्टीओमर का निर्माण होता है। स्टीरियोकैमिस्ट्री में न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रियाओं के परिणामों की भविष्यवाणी करने के लिए इस अवधारणा को समझना महत्वपूर्ण है। | |||
==अभ्यास प्रश्न== | |||
*द्विआण्विक नाभिकरागी [[प्रतिस्थापन अभिक्रिया]] से आप समझते हैं ? | |||
*एकाण्विक नाभिकरागी प्रतिस्थापन अभिक्रिया से आप समझते हैं ? | |||
*विन्यास का प्रतिलोमन किस प्रकार की अभिक्रिया में होता है? | |||
Latest revision as of 13:08, 31 May 2024
विन्यास का प्रतिलोमन स्टीरियोकेमिस्ट्री में एक महत्वपूर्ण अवधारणा है जो रासायनिक अभिक्रिया के दौरान एक काइरल केंद्र के आसपास परमाणुओं की स्थानिक व्यवस्था में परिवर्तन को संदर्भित करता है, जिसके परिणामस्वरूप मूल अणु के एक एनैन्टीओमर का निर्माण होता है। यह अवधारणा सामान्यतः न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रियाओं, विशेषकर SN2 में पाई जाती है
क्रियाविधि
विन्यास के प्रतिलोमन को समझना
काइरल केंद्र
एक कार्बन परमाणु चार अलग-अलग समूहों से बंधा होता है, जिससे गैर-सुपरइम्पोज़ेबल दर्पण छवियां (एनेंटिओमर्स) बनती हैं। रसायन विज्ञान में, कोई अणु या आयन काइरल तब कहलाता है यदि वह अणु और उसका दर्पण-प्रतिबिम्ब एक दूसरे को पूर्णतया 'ढक' न सकें। काइरलता एक अणु, आयन या किसी वस्तु में विषमता का गुण है। एक काइरल अणु वह है जिसे उसकी दर्पण छवि पर आरोपित नहीं किया जा सकता है। शब्द "काइरलता" ग्रीक शब्द "चीर" से आया है, जिसका अर्थ है "हाथ", क्योंकि काइरल अणु को प्रायः बाएं या दाएं हाथ की तरह वर्णित किया जाता है - दर्पण छवियां जिन्हें आरोपित नहीं किया जा सकता है।
काइरलता को समरूपता की कुछ विशेषताओं की कमी से परिभाषित किया गया है, जिसके कारण कोई वस्तु अपनी दर्पण छवि पर आरोपित नहीं हो पाती है। हैंडेडनेस काइरल वस्तुओं को दाएं हाथ और बाएं हाथ की वस्तुओं में वर्गीकृत करने की क्षमता से संबंधित एक अलग घटना है।
काइरल अणु
एक अणु काइरल है यदि इसमें समरूपता का आंतरिक तल नहीं है। दूसरे शब्दों में, इसकी दर्पण छवि को मूल अणु पर आरोपित नहीं किया जा सकता है। काइरलता स्टीरियोकेमिस्ट्री के क्षेत्र में एक महत्वपूर्ण अवधारणा है, जो अणुओं में परमाणुओं की त्रि-आयामी व्यवस्था का अध्ययन करती है।
न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया
एक अभिक्रिया जहां एक न्यूक्लियोफाइल कार्बन परमाणु से जुड़े एक छोड़ने वाले समूह को प्रतिस्थापित करता है। CH3Cl और हाइड्रॉक्साइड आयन की अभिक्रिया, जिसमें मेथेनॉल तथा क्लोराइड आयन बनता है यह एक द्वितीयक कोटि की अभिक्रिया है। अर्थात, अभिक्रिया का वेग दोनों अभिकारकों की सांद्रता पर निर्भर करता है। इस अभिक्रिया को आरेखीय रूप में भी प्रदर्शित किया जा सकता है।
- प्रतिस्थापन न्यूक्लियोफिलिक बिमोलेक्यूलर (SN2) अभिक्रिया एक प्रकार की कार्बनिक रासायनिक अभिक्रिया है जहां एक न्यूक्लियोफाइल (इलेक्ट्रॉन-समृद्ध प्रजाति) एक अणु में एक वाले समूह को प्रतिस्थापित करती है, जिससे एक नए रासायनिक बंध का निर्माण होता है। "द्विआणविक" पहलू इस तथ्य को संदर्भित करता है कि अभिक्रिया के दर-निर्धारण चरण में दो अणुओं का टकराव सम्मिलित है।
- SN2 अभिक्रियाएं स्टीरियोस्पेसिफिक होती हैं, जिसका अर्थ है कि वे प्रतिस्थापन के दौर से गुजर रहे कार्बन केंद्र में स्टीरियोकैमिस्ट्री के व्युत्क्रम के साथ आगे बढ़ती हैं। ऐसा इसलिए होता है क्योंकि न्यूक्लियोफाइल छोड़ने वाले समूह के विपरीत पक्ष से हमला करता है, जिससे कॉन्फ़िगरेशन का सीधा उलटा होता है।
- न्यूक्लियोफाइल इलेक्ट्रोफिलिक कार्बन परमाणु पर उस समय हमला करता है जब निकलने वाला समूह प्रस्थान करता है। इसका परिणाम एक संक्रमण अवस्था में होता है जहां न्यूक्लियोफाइल और छोड़ने वाला समूह दोनों आंशिक रूप से केंद्रीय कार्बन परमाणु से बंधे होते हैं।
अभिक्रिया दर
SN2 अभिक्रियाओं की दर न्यूक्लियोफाइल और सब्सट्रेट दोनों की सांद्रता पर निर्भर करती है, साथ ही अभिक्रियाशील कार्बन परमाणु के आसपास स्टेरिक बाधा पर भी निर्भर करती है। सामान्यतः SN2 अभिक्रिया धीमी गति से गुजरते हैं।
द्विअणुक नाभिकरागी प्रतिस्थापन को प्रदर्शित करता है। आक्रमणकारी नाभिकरागी की एल्किल हैलाइड से अन्योन्य क्रिया होने पर कार्बन और हैलोजन के मध्य का बंध टूटता है तथा कार्बन एवं आक्रमणकारी नाभिकरागी के मध्य एक नया आबंध बनता है। ये दोनों प्रक्रियाएं एक साथ एक ही पद में संपन्न होती हैं तथा कोई मध्यवर्ती नहीं बनता। जब अभिक्रिया प्रगति है तब आने वाले नाभिकरागी एवं कार्बन परमाणु के मध्य आबंध बनना प्रारम्भ हो जाता है। फिर क्रियाधार के कार्बन हाइड्रोजन बंध आक्रमणकारी नाभिकरागी से लगते हैं जब नाभिकरागी कार्बन के समीप पहुँचता है तब बंध पहले की दिशा में अग्रसर होते रहते हैं जब तक टूटने वाला समूह कार्बन से टूटकर अलग नहीं हो जाता परिणामस्वरूप आक्रमण के लिए उपलब्ध कार्बन परमाणु का विन्यास पलट जाता है और अवशिष्ट समूह बाहर निकल जाता है। इस प्रक्रिया को विन्यास का प्रतीपन कहते हैं।
विन्यास का प्रतिलोमन तब होता है जब एक रासायनिक अभिक्रिया के दौरान एक काइरल केंद्र के चारों ओर परमाणुओं की स्थानिक व्यवस्था उलट जाती है। SN2 तंत्र, यह उलटा न्यूक्लियोफाइल के पीछे के हमले के कारण होता है, जिसके परिणामस्वरूप विपरीत एनैन्टीओमर का निर्माण होता है। स्टीरियोकैमिस्ट्री में न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रियाओं के परिणामों की भविष्यवाणी करने के लिए इस अवधारणा को समझना महत्वपूर्ण है।
अभ्यास प्रश्न
- द्विआण्विक नाभिकरागी प्रतिस्थापन अभिक्रिया से आप समझते हैं ?
- एकाण्विक नाभिकरागी प्रतिस्थापन अभिक्रिया से आप समझते हैं ?
- विन्यास का प्रतिलोमन किस प्रकार की अभिक्रिया में होता है?